Kandungan
- Perbezaan Utama
- Protonasi vs Deprotonation
- Carta Perbandingan
- Apakah Protonasi?
- Apakah deprotonasi?
- Perbezaan Utama
- Kesimpulannya
Perbezaan Utama
Perbezaan utama antara protonasi dan deprotonasi adalah bahawa protonasi adalah penambahan proton dalam sebatian kimia, sedangkan deprotonasi adalah penghapusan proton daripada sebatian kimia.
Protonasi vs Deprotonation
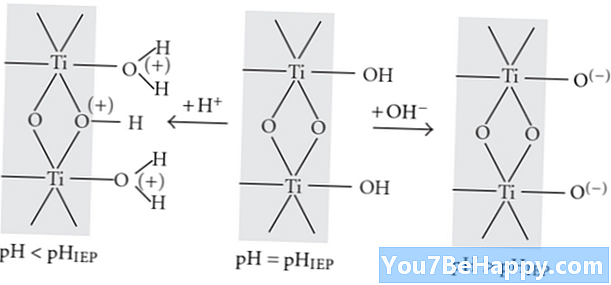
Protonasi adalah proses kimia yang berlaku semasa tindak balas kimia di mana proton menambah dalam sebatian kimia; Sebaliknya, deprotonasi adalah proses yang berlaku semasa reaksi kimia di mana proton menghilang dari sebatian kimia. Protonasi adalah peningkatan caj +1 dalam atom, molekul, ion, atau sebatian; Sebaliknya, deprotonasi adalah penurunan dalam cas +1, atom, molekul, atau sebatian.
Atom, molekul, atau sebatian yang terlibat dalam proton dipanggil asas; di sebelah flip, atom, molekul atau sebatian yang terlibat dalam deprotonasi dipanggil asid. Protonasi adalah proses di mana pH sebatian kimia meningkat; Sebaliknya, deprotonasi adalah proses di mana pH larutan suatu senyawa kimia menurun.
Protonasi adalah proses tambahan, sedangkan deprotonasi adalah penghapusan atau penghapusan proses. Protonasi adalah proses kimia di mana tenaga ditambah dalam reaksi kimia; di sebelah flip; deprotonasi adalah proses kimia di mana tenaga yang dikeluarkan semasa reaksi. Dengan kata lain, protonasi adalah penambahan H+ dalam sebatian kimia; Sebaliknya, deprotonasi adalah penghapusan H+ dari sebatian kimia.
Protonasi meningkatkan caj atom, ion, atau molekul; pada sisi flip, deprotonasi mengurangkan caj ion, atom atau molekul. Pas sentiasa menjalani proses kimia protonasi semasa tindak balas asid-asas; Sebaliknya, asid selalu menjalani proses kimia deprotonasi semasa reaksi berasaskan asid.
Protonasi adalah proses kimia menghasilkan asid konjugate semasa proses kimia; di sebelah flip; deprotonasi adalah proses kimia menghasilkan asas konjugasi semasa proses kimia. Protonasi sentiasa menyebabkan pengeluaran molekul air dari kumpulan hidroksil sebatian dalam proses kimia; pada sisi lain, deprotonasi selalu menyebabkan pengeluaran molekul hidroksil dari molekul air dalam proses kimia.
Protonasi adalah proses kimia yang sangat cepat semasa reaksi organik; Sebaliknya, deprotonasi adalah proses yang sangat lambat semasa reaksi organik. Protonasi adalah proses kimia yang merangsang proses isomerisasi, sedangkan proses kimia yang merangsang proses isomerisasi. Protonasi adalah peningkatan kadar sifat berasid; di sisi lain, deprotonasi adalah peningkatan kadar watak asas.
Carta Perbandingan
| Protonasi | Deprotonation |
| Protonasi adalah penambahan proton dalam sebatian kimia. | Deprotonasi adalah penghapusan proton daripada sebatian kimia. |
| Proton | |
| Proton menambah dalam sebatian | Proton mengeluarkan dari sebatian |
| Caj | |
| Ia meningkatkan caj +1 pada molekul | Ia mengurangkan caj +1 pada molekul |
| Kadar Keasidan atau Dasar | |
| Kadar asas | Kadar keasidan |
| PH Senyawa tersebut | |
| Ia meningkatkan pH sebatian | Ia mengurangkan pH sebatian |
| Kelajuan Proses | |
| Ia adalah proses yang cepat | Ia adalah proses perlahan |
| Proses Isomerisasi | |
| Merangsang proses isomerisasi | Menghalang proses isomerisasi |
| Tenaga Proses | |
| Ia menambah tenaga kepada tindak balas | Ia mengeluarkan tenaga dari reaksi |
| Jenis Proses | |
| Proses tambahan | Menghapuskan proses |
| H+ Ion | |
| Ion hidrogen menambah dalam sebatian | Ion hidrogen menghapuskan dari sebatian |
| Kemaskini | |
| Ia adalah proses yang boleh diterbalikkan | Ia adalah proses yang tidak dapat dipulihkan |
| Keupayaan Catalytic | |
| Ia mempunyai kuasa pemangkin | Ia tidak mempunyai kuasa pemangkin |
Apakah Protonasi?
Protonasi adalah proses kimia penambahan proton dalam sebatian kimia semasa tindak balas kimia. Ini adalah proses yang sangat cepat. Ia boleh membentuk molekul air dari molekul hidroksil. Protonasi adalah proses yang boleh diterbalikkan yang meningkatkan caj sebatian kimia dengan kadar caj +1 dalam atom, ion, molekul, atau spesies.
PH penyelesaian atau pelarut yang terlibat dalam protonasi adalah sangat rendah. Protonasi adalah kadar asas atau keasaman bahan kimia atau organik. Protonasi adalah proses tambahan atau endotermik yang terlibat dalam proses isomerisasi. Ia juga merangsang proses pempolimeran.
Ia mempunyai kuasa pemangkin untuk meningkatkan keasidan tindak balas yang digunakan dalam beberapa proses seperti tindak balas tambahan, tindak balas nukleofilik, elektrofilik, reaksi penggantian, dan sebagainya. Proses protonasi adalah berkadar dengan tahap sifat asidat bahan tersebut. Biasanya ia melibatkan pembentukan molekul air semasa proses.
Ion hidrogen sentiasa ditambah dalam sebatian kimia semasa proses protonasi. Ia juga mempunyai keupayaan untuk mengubah ciri-ciri optik molekul. Proses protonasi sebatian bergantung kepada keasidan asid yang tersedia untuk penyelesaian atau pelarut. Proses protonasi digunakan untuk mengurangkan kereaktifan molekul organik. Protonasi umumnya dikenali sebagai proses endoterik yang melibatkan melepaskan tenaga dengan mendermakan proton kepada spesies kimia dengan mudah.
Proses seperti penambahan hidrogen dalam molekul ammonia yang menghasilkan pembentukan ion amonium, penambahan ion hidrogen dalam molekul air untuk menghasilkan ion hidronium, protonasi ion hidroksil untuk membentuk molekul air, penambahan ion hidrogen kepada alkohol untuk membentuk ion hidronium dalam larutan, penambahan ion hidrogen ke alkena dan alkena, dan lain-lain yang paling baik menjelaskan protonasi istilah.
Apakah deprotonasi?
Deprotonation adalah proses kimia menghilangkan proton dari sebatian kimia semasa tindak balas kimia. Ia adalah proses perlahan. Proses ini juga mempunyai keupayaan untuk membentuk ion hidroksil dari molekul air. Deprotonation adalah proses tak dapat dipulihkan yang mempunyai keupayaannya untuk mengurangkan caj sebatian kimia dengan kadar caj +1 dalam atom, molekul, atau spesies ion.
PH penyelesaian atau pelarut yang terlibat dalam proses deprotonasi sangat tinggi. Proses ini tidak mempunyai keupayaan untuk melakukan tindak balas kimia dengan bertindak sebagai pemangkin. Proses protonasi adalah berkadar dengan sifat asas bahan tersebut. Ion hidrogen sentiasa menghilangkannya dari sebatian kimia semasa proses deprotonasi. Aktiviti optiknya juga berubah-ubah.
Proses deprotonasi juga bergantung kepada pH penyelesaian atau pelarut. Proses ini meningkatkan kereaktifan molekul organik. Proses seperti penyingkiran ion hidrogen dari air untuk membentuk ion hidroksil, penyingkiran proton daripada alkana untuk membentuk alkenes dan alkena, penyingkiran ion hidrogen dari alkohol, dan lain-lain. Menjelaskan terbaik istilah deprotonasi.
Perbezaan Utama
- Protonasi adalah fenomena tambahan proton; Sebaliknya, deprotonasi adalah fenomena penyingkiran proton.
- Protonasi sentiasa meningkatkan pH penyelesaian kimia; di sebelah flip, deprotonasi sentiasa menurunkan pH penyelesaian kimia.
- Protonasi sentiasa menambah caj +1 ke sebatian kimia; Sebaliknya, deprotonasi sentiasa membuang caj +1 ke sebatian kimia.
- Protonasi adalah peningkatan kadar sifat berasid; di sisi lain, deprotonasi adalah peningkatan kadar watak asas.
- Protonasi berlaku sangat cepat; Sebaliknya, deprotonasi berlaku dengan perlahan.
- Bas umumnya digunakan dalam proses protonasi dengan menerima proton; sebaliknya; deprotonasi yang biasanya digunakan dalam proses deprotonasi dengan mengeluarkan proton.
- Penambahan tenaga berlaku dalam proses protonasi; di sebelah belakang, penyingkiran tenaga berlaku dalam proses deprotonasi.
- Protonasi meningkatkan caj atom, ion, atau molekul; pada sisi flip, deprotonasi mengurangkan caj ion, atom atau molekul.
- Proses protonasi melibatkan dalam isomerisasi bahan kimia; Sebaliknya, proses deprotonasi tidak melibatkan dalam isomerisasi bahan kimia.
- Protonasi adalah proses kimia yang berlaku di pangkalan semasa tindak balas asid-asas; pada flip side, deprotonation adalah proses kimia yang terjadi di asid semasa reaksi asid-base.
- Protonasi sentiasa menghasilkan asid conjugate dalam proses kimia; Sebaliknya, deprotonasi selalu menghasilkan asas konjugasi dalam proses kimia.
- Protonasi menjadikan penyelesaian itu lebih tertumpu; di sebelah flip, deprotonasi menjadikan penyelesaian kurang tertumpu.
- Protonasi melibatkan dalam pembuatan molekul air; Sebaliknya, deprotonasi melibatkan dalam pembuatan molekul hidroksil.
- Protonasi adalah proses endoterik; Sebaliknya, deprotonasi adalah proses eksotermik.
Kesimpulannya
Perbincangan di atas menyimpulkan bahawa protonasi adalah kenaikan caj +1 bahan kimia; Sebaliknya, deprotonasi adalah pengurangan dalam cas +1 pada sebatian kimia.